Derivati del benzene |
|---|
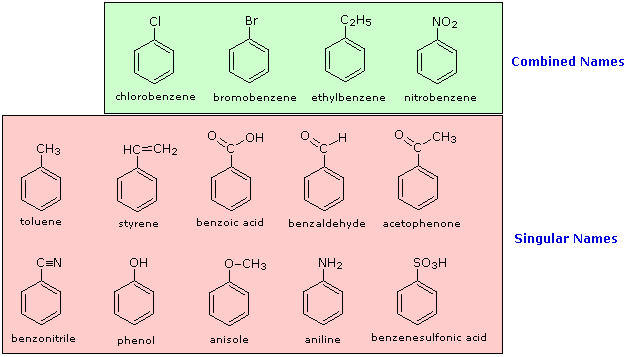
La nomenclatura dei composti di sostituzione dell'anello benzenico č meno sistematica di quella degli alcani, alcheni e alchini. Pochi composti monosostituiti sono denominati usando un nome di un gruppo quale prefisso a "benzene", come mostrato dall'elenco seguente di nomi combinati. Alla maggior parte di questi composti, tuttavia, ci si riferisce con nomi particolari che sono univoci. Non esiste una alternativa semplice per imparare a memoria in studi di approfondimento questi nomi.

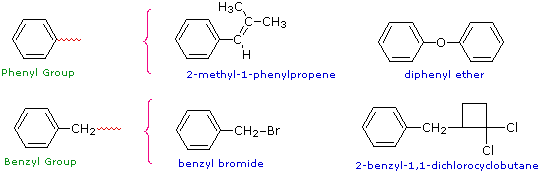
Due gruppi sostituenti incontrati comunemente che incorporano un anello benzenico sono i fenili, e i benzili. Questi sono qui mostrati con esempi del loro uso. Bisogna essere attenti a non confondere un gruppo fenile con il composto fenolo. Una notazione generale ed utile, complementare all'uso di R- per un gruppo alchilico, č Ar- per un gruppo arilico (qualunque anello aromatico).
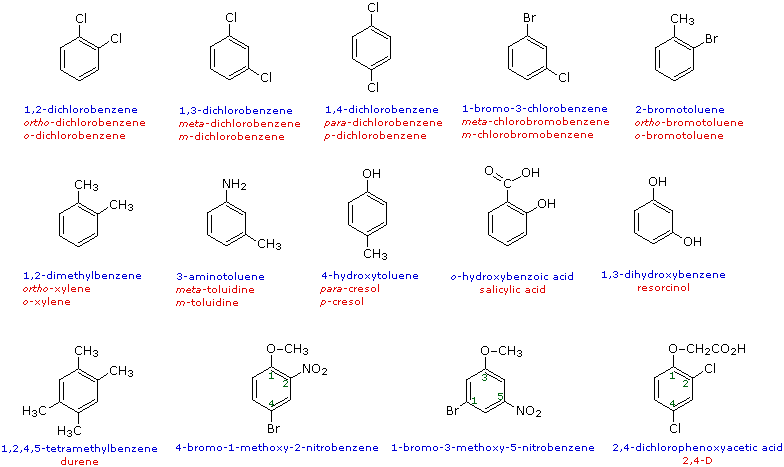
Quando č presente piů di un sostituente su un anello benzenico, le localizzazioni relative dei sostituenti possono essere designate numerando gli atomi di carbonio dell'anello o attraverso qualche altra notazione. Nel caso di benzeni bisostituiti, sono comunemente utilizzati i prefissi orto, meta e para rispettivamente una relazione 1,2- o 1,3- o 1,4-. Negli esempi seguenti, la prima riga di composti mostra questo uso in colore rosso. Alcuni tolueni disostituiti hanno nomi particolari (per es. xilene, cresolo e toluidina) ed i loro isomeri sono normalmente designati dai prefissi orto-, meta- o para-. Pochi benzeni bisostituiti hanno nomi particolari assegnati ad isomeri specifici (ad es. acido salicilico e resorcinolo). Infine, se vi sono tre o piů gruppi sostituenti, l'anello č numerato in maniera tale da assegnare ai sostituenti i numeri piů piccoli possibili, come illustrato dall'ultima riga degli esempi. I sostituenti sono elencati nel nome finale in ordine alfabetico. Se la sostituzione č simmetrica (terzo esempio dalla sinistra) la numerazione corrisponde all'ordine alfabetico.